在製藥行業(ye) ,合規性要求是企業(ye) 的生命線。隨著製藥行業(ye) 信息化、數字化及自動化技術的不斷引進,計算機化係統驗證(CSV)的標準與(yu) 要求也在持續更新及加嚴(yan) 。在強合規監管下如何全麵有效地落實CSV,是所有製藥企業(ye) 必須要解決(jue) 的難題。
CSV法規對製藥企業(ye) 至關(guan) 重要,各國法規/指南均明確提出:在製藥和生命科學相關(guan) 法規中,當計算機化係統代替人工操作時,應當確保此類係統符合相關(guan) 法規要求。美國FDA、歐盟Annex11、歐盟EMA、中國CFDA等都對計算機化係統驗證做了重點要求
G22恒峰CSV服務:體(ti) 係化服務·全流程驗證
為(wei) 滿足製藥企業(ye) 的合規需求,G22恒峰智慧充分發揮在製藥自動化、信息化領域的產(chan) 品技術優(you) 勢與(yu) 項目管理經驗,結合中國CFDA、歐盟EMA、美國FDA等法規的重點要求,為(wei) 有GMP/FDA/EUGMP認證需求的製藥企業(ye) 提供合規、優(you) 質、快捷的CSV服務,由多名行業(ye) 資深技術人員組成的驗證團隊製定並執行全麵科學的代碼審核、功能測試、係統驗證等方案,護航製藥企業(ye) 合規發展。
體(ti) 係化服務
用戶需求說明:用戶需求說明(URS)需要清晰而準確的定義(yi) 出係統所有預期需要實現的功能,是供應商編寫(xie) 功能設計說明(FDS)的基礎。G22恒峰CSV服務可為(wei) 客戶輔助完善URS內(nei) 容。
風險評估:風險評估過程界定出了用於(yu) 控製對GMP要求或客戶業(ye) 務有影響的風險的必要措施。必須確定出這些風險並對其進行評估、文件記錄。
驗證計劃:計劃關(guan) 注的重點是患者安全、產(chan) 品質量和數據的完整性。並整個(ge) 項目進行總結,找出成功的措施。
質量項目計劃:質量項目計劃(QPP)是一個(ge) 界定了項目的生命周期,規定出了為(wei) 了滿足用戶質量要求所提議采取的方法,使各項項目工作符合控製規程要求的文件。
功能設計說明:功能設計說明是一個(ge) 界定了如何用以滿足在用戶需求說明中所規定的客戶功能要求的文件,供應商對URS的一個(ge) 在功能和技術上所做的響應,也是工廠驗收測試(FAT)的主要基礎。
軟件設計說明:定義(yi) 出具體(ti) 功能要求後,依據要求如何配置軟件、配置哪些軟件以及這些軟件如何去滿足功能要求的一個(ge) 設計型文件,它是工廠驗收測試(FAT)中軟件測試的基礎。
設計確認:DQ是用以證明係統的軟硬件設計能夠滿足用戶需求和功能要求。它由供應商來編寫(xie) 方案並完成報告,需用戶進行審查和批準。
工廠驗收測試:工廠驗收測試是自控係統實施完成之後在供應商的工廠進行的,作為(wei) 供應商發貨標準和依據的確認性文件。
安裝確認:確認控製係統的安裝符合設計要求及用戶需求,確認係統(包括一些傳(chuan) 感器、執行器)是否按照係統說明及生產(chan) 工藝要求進行安裝,設備性能是否滿足產(chan) 品質量指標控製水平。
運行確認:確認控製係統已經按照URS要求和設計要求能夠正常運行。確認對該係統的每一部分及整體(ti) 進行功能試驗,檢查和核實係統能在要求範圍內(nei) 準確運行並達到規定的技術指標。
係統權限:提供或協助企業(ye) 製定權限管理SOP和權限矩陣。
審計追蹤:審計追蹤一旦生成不可修改,不可刪除,能夠記錄誰、在什麽(me) 時間、因為(wei) 什麽(me) 、做了什麽(me) 。
電子簽名:提供符合聯邦法規21章11款要求的電子簽名。
追溯矩陣:對係統的用戶需求和測試內(nei) 容之間的聯係進行總結。
驗證報告:驗證報告(VR)是對自控係統整個(ge) 驗證生命周期所做的工作結果的總結性質的報告文件。它由供應商來編寫(xie) ,需要客戶進行批準,是對驗證計劃(VP)或質量項目計劃(QPP)的一個(ge) 對應回顧。
培訓:在所有的測試開始之前,G22恒峰驗證工程師會(hui) 在每個(ge) 階段對參與(yu) 測試的人員進行關(guan) 於(yu) 本次測試內(nei) 容的培訓。
全流程驗證
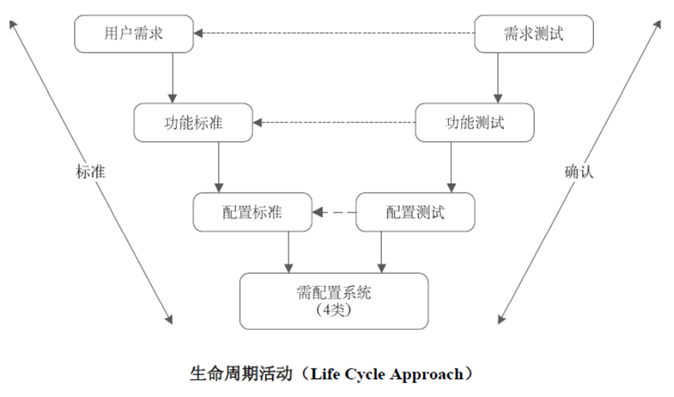
藥監總局發布的關(guan) 於(yu) 《藥品生產(chan) 質量管理規範(2010年修訂)》中關(guan) 於(yu) 計算機係統驗證(CSV)的內(nei) 容,明確了計算機係統驗證應該貫穿於(yu) 計算機化係統生命周期的全過程。
例如溫度控製流程,就是計算機係統需要通過驗證進行確認的預期用途。如果隻驗證計算機係統, 而不驗證其預期用途,無法知道流程是否能夠正確運行。例如對生產(chan) 執行係統平台進行確認,能保證它符合標準要求,但不能證明該平台生成的主生產(chan) 記錄和檢驗記錄中包含的計算是正確的。在此例中,對流程進行驗證則可確保主生產(chan) 記錄和檢驗記錄中預期的步驟,標準要求和計算均是正確的。
以國內(nei) 某大型製藥集團企業(ye) 自控項目為(wei) 例,該企業(ye) 要求自控係統可實現反應釜溫度、壓力在線監測自動控製以及報警聯鎖、危險原料進料監測及控製、儲(chu) 罐液位控製等自動控製過程管理,包括硬件、軟件、功能、安裝等方麵,以及GMP驗證的服務。

在滿足自控需求的基礎上,G22恒峰提供了前期的技術支持。項目前期,由於(yu) 業(ye) 主未確定設計院,G22恒峰CSV服務團隊應該企業(ye) 要求對自控改造方麵提出建議。在合規的情況下,幫助其對自控點位進行優(you) 化,在原有P&ID工藝流程圖的基礎上,完成了自控改造的優(you) 化建議。並配合完成供應商評估,確保資質與(yu) 能力的符合性;配合對URS內(nei) 容調整,保證自控係統可靠性和合規性。通過在項目前期便介入的CSV服務,確保了項目順利通過FDA認證。

截至目前,圍繞製藥行業(ye) 自動化、信息化以及CSV等建設需求,G22恒峰已與(yu) 業(ye) 內(nei) 眾(zhong) 多百強企業(ye) 達成合作,為(wei) 製藥企業(ye) 全麵合規的智造轉型升級提供一站式技術產(chan) 品與(yu) 服務。
通過G22恒峰提供的完整合規的CSV服務,不僅(jin) 能滿足製藥企業(ye) 的GMP/FDA/EUGMP認證需求。同時還能確保計算機化係統工程符合預期要求,保障生產(chan) 過程和藥品質量安全,並保持持續的驗證狀態。
從(cong) 製造到“智造”,計算機化係統在製藥行業(ye) 的應用將愈加廣泛與(yu) 複雜,G22恒峰將不斷改進並完善CSV服務,持續滿足製藥企業(ye) 對計算機化係統的合規需求,助力製藥企業(ye) 轉型升級!






